要点提炼:
合并高危复发因素肝内胆管癌患者:肿瘤直径 >5 cm、血管侵犯、多发病灶、肝门区淋巴结转移及CA19-9升高等
建议行新辅助治疗3周期:3个周期特瑞普利单抗+仑伐替尼+吉西他滨+奥沙利铂(GOLP)联合治疗
达到效果后,于2~4周内行根治性切除并行肝门区淋巴结清扫,术后予卡培他滨辅助治疗8周期(6个月左右)
未来方向:将ICC结果推广至具备高危因素的胆管癌患者,尤其胆囊癌,肝门部胆管癌,围术期三明治(新辅助+手术+辅助治疗)能取得更大效果。
作为患者,心理追求快速手术反而不好,耐心接受新辅助治疗!
今晨,《新英格兰医学杂志》(NEJM)发表由复旦大学附属中山医院樊嘉院士、周俭院士和施国明教授团队完成的新辅助治疗可切除高危肝内胆管癌论著。
这项由研究者发起的名为ZSAB-neoGOLP的2~3期随机对照试验共纳入178例有高复发风险因素、可切除的肝内胆管癌患者(新辅助组88例,对照组90例),新辅助组采用免疫检查点抑制剂特瑞普利单抗+抗血管生成药仑伐替尼+化疗药物吉西他滨-奥沙利铂新辅助治疗(新辅助GOLP方案),对照组直接行手术。所有患者术后接受卡培他滨辅助治疗。结果表明,新辅助治疗显著改善患者无病生存期(新辅助组 vs. 对照组,18.0个月 vs. 8.7个月;P<0.001)。

ZSAB-neoGOLP研究:
从“可切除”走向“生物学控制”的治疗范式转变
肝内胆管癌(ICC)是仅次于肝细胞癌的第二常见原发性肝恶性肿瘤,其全球发病率呈持续上升趋势。与多数实体肿瘤类似,ICC的核心挑战并非“能否手术切除”,而是即便切除,复发风险仍然较高。既往研究提示:仅约三分之一患者在初诊时具备手术机会;而在接受以根治为目的切除后,复发率仍超过50%,五年生存率仅约30%。
尤其是在“可切除”的人群中,若合并肿瘤体积大、血管侵犯、多发病灶、肝门区淋巴结转移或CA19-9升高等肿瘤侵袭性较高的特征,许多患者在术后一年内即出现早期复发或远处转移。这一临床困境使得传统“直接手术”的路径面临严峻挑战。
今晨,《新英格兰医学杂志》(NEJM)发表的ZSAB-neoGOLP研究首次以随机对照研究的形式,为高危可切除ICC的新辅助治疗提供了关键循证证据,具有里程碑意义。
为什么ICC迫切需要新辅助治疗?
从肿瘤生物学角度来看,新辅助治疗在高危ICC中具有三重潜在价值:
1. 提前清除微转移灶,降低早期复发风险;
2. 重塑肿瘤免疫微环境,提高全身治疗敏感性;
3. 通过治疗应答对不同肿瘤生物学行为患者进行筛选,优化手术决策。
然而,既往ICC新辅助研究多为回顾性队列研究或单臂探索性研究(如NEO-GAP、NEO-ERA-01),缺乏随机对照证据支持其标准化应用。随着晚期ICC中“化疗+免疫+抗血管生成”疗效的逐步显现,将全身治疗前移至围手术期以降低早期复发风险,成为合理且迫切的研究方向。
研究设计亮点:精准锁定“高危可切除人群”, 无缝2~3期设计
ZSAB-neoGOLP为多中心、开放标签、随机对照、无缝2~3期试验,共纳入178例高危可切除ICC患者。其最具创新性的设计在于:精准定义高复发风险人群,仅纳入具备至少一项高危因素的患者,包括肿瘤直径 >5 cm、血管侵犯、多发病灶、肝门区淋巴结转移及CA19-9升高等。这一策略避免了既往研究中风险层级混杂的问题,使研究结果更贴近真实临床“高危决策场景”。
入组患者随机分配,新辅助组接受3个周期特瑞普利单抗+仑伐替尼+吉西他滨+奥沙利铂(GOLP)联合治疗;完成后经多学科团队(MDT)评估,于2~4周内行根治性切除并行肝门区淋巴结清扫。对照组则直接手术。两组患者术后均接受8个周期卡培他滨辅助治疗。
研究主要终点为无事件生存(EFS),次要终点包括总生存(OS)、客观缓解率(ORR)、R0切除、主要病理学缓解(MPR)、病理学完全缓解(pCR)、无复发生存期以及安全性等。该试验设计两次期中分析,采用α消耗函数控制I类错误,统计学设计严谨。
主要结果:EFS显著延长,临床意义明确
在预设期中分析(中位随访16.9个月)时,新辅助GOLP组显示出显著疗效优势:新辅助治疗组与对照组的中位EFS分别为18.0个月和8.7个月;2年EFS率分别为37%和25%(P<0.001)。
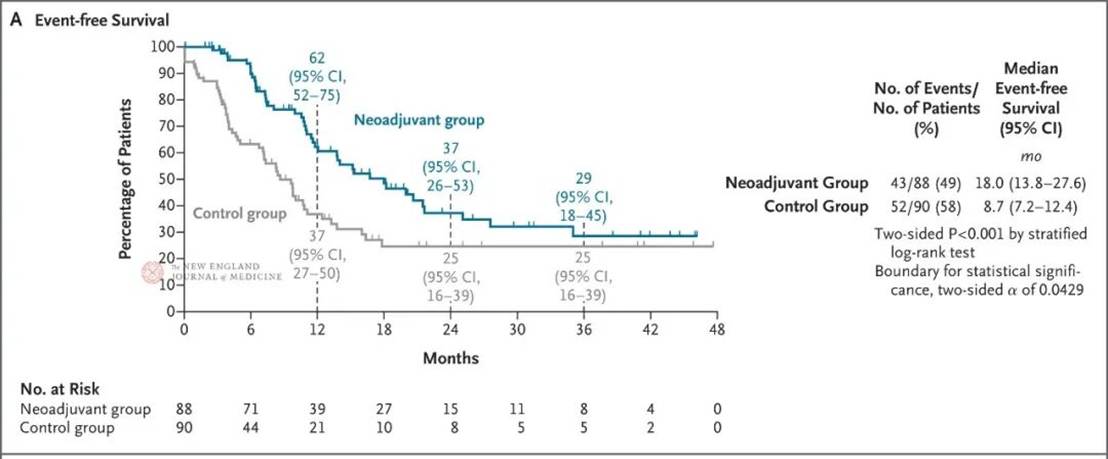
图1. 期中分析的无事件生存结果。
对于以“术后早期复发”为主要失败模式的肿瘤而言,EFS延长约6.6个月具有较高的临床价值。同时,对照组中位EFS仅8.7个月,真实揭示了高危可切除ICC在传统治疗路径下的预后困境。
OS趋势积极,但期中证据尚不足以“盖棺定论”
期中分析显示:新辅助组与对照组24个月OS率分别为79% vs. 61%(HR,0.43;95% CI,0.23~0.79;P=0.005),虽然尚未达到预设的统计学阈值,但总体生存获益趋势明确。随着随访时间延长,OS结果有望进一步巩固其临床价值。
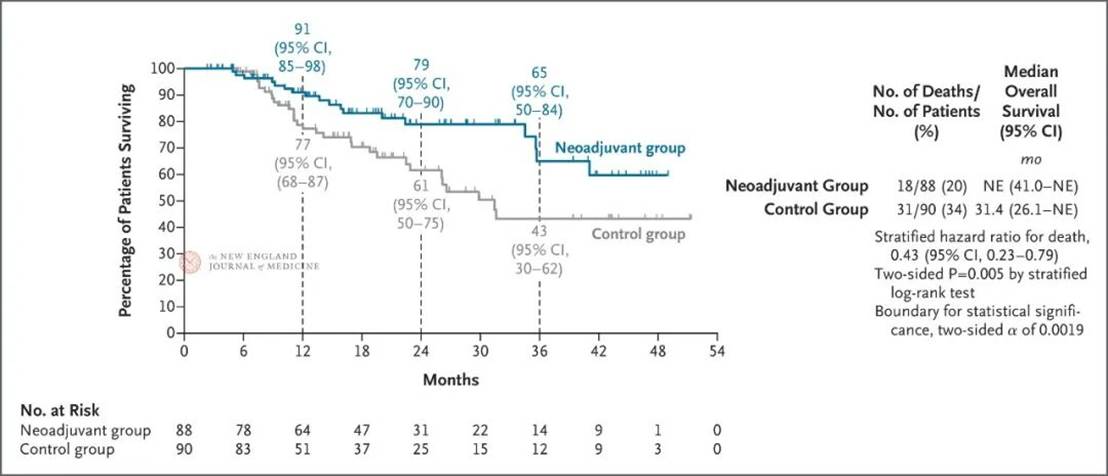
图2. 期中分析的总生存结果。
病理学缓解:不仅“缩瘤”,更是“控制生物学行为”
次要终点方面,新辅助GOLP治疗组的ORR达55%,MPR为19%,pCR率为5%,而且R0切除率高达95%。相比既往研究,尽管主要病理缓解率并不太高,但其与EFS改善高度一致,提示新辅助治疗的核心价值可能并不局限于肿瘤缩小,而在于对微转移及肿瘤生物学行为的系统性控制——这一点对于ICC尤为关键。
安全性:毒性可控,不影响手术实施
安全性数据同样显示了该方案的临床可操作性:新辅助治疗阶段,≥3级不良事件发生率为28%,≥3级治疗相关不良事件为26%,以中性粒细胞减少、白细胞减少等骨髓抑制为主。免疫相关不良事件发生率为36%(以甲减、皮疹为主)。无治疗相关死亡;手术并发症发生率与对照组相当。
总体来看,毒性谱与既往研究一致,未观察到影响手术可行性的安全信号,为围手术期应用提供了重要安全依据。
外科视角的关键启示:治疗重心正在前移
对于外科医生而言,这项研究的真正价值在于理念层面的改变:高危ICC的预后,决定因素不再是“是否能切除”,而是“是否在手术前已控制疾病生物学”:传统路径:直接手术 → 术后复发 → 被动补救治疗;未来可能的优化路径:新辅助全身治疗 → 精准外科切除 → 个体化辅助治疗。这意味着外科决策将从“技术可切除性评估”升级为“生物学可获益性评估”,也更加契合现代肿瘤综合治疗理念。
未来研究版图:围手术期全身治疗正成为研究热点
从全球临床试验布局看,高危可切除ICC的围手术期治疗已成为前沿方向。多项研究正探索免疫治疗联合化疗±抗血管生成治疗作为新辅助或围手术期治疗策略,例如PD-1/PD-L1联合吉西他滨+顺铂(GemCis方案)、免疫+TKI+化疗三联方案,以及区域治疗(如肝动脉灌注化疗)联合免疫治疗等。这些试验普遍聚焦具有高复发风险特征的可切除人群,并以EFS、R0切除率及病理缓解作为关键终点。
值得注意的是,当前研究设计呈现两个共同趋势:一是精准界定“高危可切除”亚群,二是将全身治疗前移至术前阶段以实现早期生物学控制。ZSAB-neoGOLP的阳性结果,与这一全球研究方向高度一致,进一步强化了“围手术期综合治疗”可能成为未来高危ICC标准路径的理论基础。
结语:ICC围手术期治疗有了循证证据
长期以来,高危可切除ICC处于“手术可做但预后不佳”的灰色地带。ZSAB-neoGOLP研究首次采用随机对照试验证明,新辅助三联四药GOLP方案可显著延长EFS,具有重要的临床实践意义。尽管OS仍需随访验证,但其里程碑意义已然明确:ICC围手术期治疗正从“以手术为中心”走向“以疾病生物学控制为核心”的循证整合阶段。对于高危可切除ICC患者而言,这或许标志着一个全新的治疗时代正在开启。